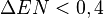La afinidad electrónica (AE) o electroafinidad se define como la energía involucrada cuando un átomo gaseoso neutro en su estado fundamental (de mínima energía) captura un electrón y forma un ion mononegativo:
 .
.Dado que se trata de energía liberada, pues normalmente al insertar un electrón en un átomo predomina la fuerza atractiva del núcleo, tiene signo negativo. En los casos en los que la energía sea absorbida,cuando ganan las fuerzas de repulsión,tendrán signo positivo;AE se expresa normalmente en kJmol-1.
También podemos recurrir al proceso contrario para determinar la primera afinidad electrónica, ya que sería la energía consumida en arrancar un electrón a la especie aniónica mononegativa en estado gaseoso de un determinado elemento; evidentemente la entalpía correspondiente AE tiene signo negativo, salvo para los gases nobles y metales alcalinotérreos.Este proceso equivale al de la energía de ionización de un átomo, por lo que la AE sería por este formalismo la energía de ionización de orden cero.
Esta propiedad nos sirve para prever que elementos generaran con facilidad especies aniónicas estables,aunque no hay que relegar otros factores:tipo de contraión, estado sólido, ligando-disolución,etc
La electroafinidad aumenta cuando el tamaño del átomo disminuye, el efecto pantalla no es potente o cuando decrece el nº atómico. Visto de otra manera: aumenta de izquierda a derecha, y de abajo hacia arriba, al igual que lo hace la electronegatividad. En la tabla periódica tradicional no es posible encontrar esta información.
Los elementos del bloque p,y en concreto los del grupo17, son los que tienen las mayores afinidades electrónicas, mientras que los átomos con configuraciones externas s2 (Be,Mg,Zn), s2p6 (Ne,Ar,Kr) junto con los que tienen semilleno el conjunto de orbitales p (N,P,As) son los de más baja AE.Esto último demuestra la estabilidad cuántica de estas estructuras electrónicas que no admiten ser perturbadas de forma fácil.Los elementos que presentan mayores A.E. son el flúor y sus vecinos más próximos O, S, Se, Cl y Br -aumento destacado de la carga nuclear efectiva que se define en esta zona de la T.P.-, salvo los gases nobles que tienen estructura electrónica cerrada de alta estabilidad y cada electrón que se les inserte debe ser colocado en una capa superior vacía.
Vamos a destacar algunos aspectos relacionados con la A.E. que se infieren por el puesto y zona del elemento en la T.P.:
- Los elementos situados en la parte derecha de la T.P., bloque p, son los de afinidades electrónicas favorables,manifestando su carácter claramente no metálico.
- Las afinidades electrónicas más elevadas son para los elementos del grupo 17, seguidos por los del grupo 16.
- Es sorprendente que el flúor tenga menor afinidad que el cloro, pero al colocar un electrón en el F,un átomo más pequeño que el Cl,se deben vencer fuerzas repulsivas entre los electrones de la capa de valencia.A partir del cloro la tendencia es la esperada en función de la mayor distancia de los electrones exteriores al núcleo.
- El nitrógeno tiene una afinidad electrónica muy por debajo de sus elementos vecinos, tanto del periodo como de su grupo, lo que es debido a su capa de valencia semillena que es muy estable.
- Los restantes elementos del grupo 15 si presentan afinidades electrónicas más favorables,a pesar de la estabilidad de la capa semillena, porque el aumento del tamaño hace que esa capa exterior esté separada del núcleo por otras intermedias.
- Hay que destacar también el papel del hidrógeno, ya que su afinidad no es muy alta, pero lo suficiente para generar el ión H- que es muy estable en hidruros iónicos y especies complejas. Aquí también podemos aplicar el razonamiento análogo al del flúor, porque tenemos un átomo todavía más pequeño y queremos adicionarle un electrón venciendo las fuerzas repulsivas del electrón 1s1.
- Con relación al bloque d debemos fijarnos en el caso especial del oro pues su afinidad electrónica, -223kJmol−1, es comparable a la del yodo con –295kJmol−1, con lo que es factible pensar en el anión Au-.Se han logrado sintetizar compuestos iónicos de oro del tipo RbAu y CsAu, con la participación de los metales alcalinos más electropositivos. En ellos se alcanza la configuración tipo pseudogas noble del Hg (de 6s1 a 6s2) para el ión Au- (contracción lantánida + contracción relativista máxima en el Au).
| Grupo | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| Periodo | |||||||||||||||||||
| 1 | H -73 | He 21 | |||||||||||||||||
| 2 | Li -60 | Be 19 | B -27 | C -122 | N 7 | O -141 | F -328 | Ne 29 | |||||||||||
| 3 | Na -53 | Mg 19 | Al -43 | Si -134 | P -72 | S -200 | Cl -349 | Ar 35 | |||||||||||
| 4 | K -48 | Ca 10 | Sc -18 | Ti -8 | V -51 | Cr -64 | Mn | Fe -16 | Co -64 | Ni -112 | Cu -118 | Zn 47 | Ga -29 | Ge -116 | As -78 | Se -195 | Br -325 | Kr 39 | |
| 5 | Rb -47 | Sr | Y -30 | Zr -41 | Nb -86 | Mo -72 | Tc -53 | Ru -101 | Rh -110 | Pd -54 | Ag -126 | Cd 32 | In -29 | Sn -116 | Sb -103 | Te -190 | I -295 | Xe 41 | |
| 6 | Cs -45 | Ba | Lu | Hf | Ta -31 | W -79 | Re -14 | Os -106 | Ir -151 | Pt -205 | Au -223 | Hg 61 | Tl -20 | Pb -35 | Bi -91 | Po -183 | At -270 | Rn 41 | |
| 7 | Fr -44 | Ra | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Uuq | Uup | Uuh | Uus | Uuo | |
La electronegatividad, (abreviación EN, símbolo χ (letra griega chi)) es una propiedad química que mide la capacidad de un átomo (o de manera menos frecuente un grupo funcional) para atraer hacia él los electrones, o densidad electrónica, cuando forma un enlace covalente en una molécula.[1]También debemos considerar la distribución de densidad electrónica alrededor de un átomo determinado frente a otros, tanto en una especie molecular como en un compuesto no molecular.
La electronegatividad de un átomo determinado está afectada fundamentalmente por dos magnitudes, su masa atómica y la distancia promedio de los electrones de valencia con respecto al núcleo atómico. Esta propiedad se ha podido correlacionar con otras propiedades atómicas y moleculares. Fue Linus Pauling el investigador que propuso esta magnitud por primera vez en el año 1932, como un desarrollo más de su teoría del enlace de valencia.[2] La electronegatividad no se puede medir experimentalmente de manera directa como, por ejemplo, la energía de ionización, pero se puede determinar de manera indirecta efectuando cálculos a partir de otras propiedades atómicas o moleculares.
Se han propuesto distintos métodos para su determinación y aunque hay pequeñas diferencias entre los resultados obtenidos todos los métodos muestran la misma tendencia periódica entre los elementos.
El procedimiento de cálculo más común es el inicialmente propuesto por Pauling. El resultado obtenido mediante este procedimiento es un número adimensional que se incluye dentro de la escala de Pauling. Escala que varía entre 0,7 para el elemento menos electronegativo y 4,0 para el mayor.
Es interesante señalar que la electronegatividad no es estrictamente una propiedad atómica, pues se refiere a un átomo dentro de una molécula[3] y, por tanto, puede variar ligeramente cuando varía el "entorno"[4] de un mismo átomo en distintos enlaces de distintas moléculas. La propiedad equivalente de la electronegatividad para un átomo aislado sería la afinidad electrónica o electroafinidad.
Dos átomos con electronegatividades muy diferentes forman un enlace iónico. Pares de átomos con diferencias pequeñas de electronegatividad forman enlaces covalentes polares con la carga negativa en el átomo de mayor electronegatividad.
Los diferentes valores de electronegatividad se clasifican según diferentes escalas, entre ellas la escala de Pauling anteriormente aludida y la escala de Mulliken.
En general, los diferentes valores de electronegatividad de los átomos determinan el tipo de enlace que se formará en la molécula que los combina. Así, según la diferencia entre las electronegatividades de éstos se puede determinar (convencionalmente) si el enlace será, según la escala de Linus Pauling:
Cuanto más pequeño es el radio atómico, mayor es la energía de ionización y mayor la electronegatividad y viceversa, la electronegatividad es la tendencia o capacidad de un átomo, en una molécula, para atraer hacia sí los electrones, un elemento con alta electronegatividad es altamente oxidante y puede mezclarse facilmente con otros elementos de menor electronegatvidad. Ni las definiciones cuantitativas ni las escalas de electronegatividad se basan en la distribución electrónica, sino en propiedades que se supone reflejan la electronegatividad. La electronegatividad de un elemento depende de su estado de oxidación y, por lo tanto, no es una propiedad atómica invariable. Esto significa que un mismo elemento puede presentar distintas electronegatividades dependiendo del tipo de molécula en la que se encuentre, por ejemplo, la capacidad para atraer los electrones de un orbital híbrido spn en un átomo de carbono enlazado con un átomo de hidrógeno, aumenta en consonancia con el porcentaje de carácter s en el orbital, según la serie etano < etileno(eteno) < acetileno(etino). La escala de Pauling se basa en la diferencia entre la energía del enlace A–B en el compuesto ABn y la media de las energías de los enlaces homopolares A–A y B–B.R. S. Mulliken propuso que la electronegatividad de un elemento puede determinarse promediando la energía de ionización de sus electrones de valencia y la afinidad electrónica. Esta aproximación concuerda con la definición original de Pauling y da electronegatividades de orbitales y no electronegatividades atómicas invariables.
La escala Mulliken (también llamada escala Mulliken-Jaffe) es una escala para la electronegatividad de los elementos químicos, desarrollada por Robert S. Mulliken en 1934. Dicha escala se basa en la electronegatividad Mulliken (cM) que promedia la afinidad electrónica A.E. (magnitud que puede relacionarse con la tendencia de un átomo a adquirir carga negativa) y los potenciales de ionización de sus electrones de valencia P.I. o E.I. (magnitud asociada con la facilidad, o tedencia, de un átomo a adquirir carga positiva). Las unidades empleadas son el KJ/mol:
| Al 1,37 | Ar 3,36 | As 2,26 | B 1,83 | Be 1,99 | Br 3,24 | C 2,67 | Ca 1,30 | Cl 3,54 | F 4,42 | Ga 1,34 |
| Ge 1,95 | H 3,06 | I 2,88 | In 1,30 | K 1,03 | Kr 2,98 | Li 1,28 | Mg 1,63 | N 3,08 | Na 1,21 | Ne 4,60 |
| O 3,21 | P 2,39 | Rb 0,99 | S 2,65 | Sb 2,06 | Se 2,51 | Si 2,03 | Sn 1,83 | Sr 1,21 | Te 2,34 | Xe 2,59 |